Introduction
Dans l’article sur le tout ou rien, nous avions vu qu’il existait différentes méthodes pour tenter de restaurer les batteries au plomb. Nous proposons, ne faisant ainsi pas de « tout ou rien », une méthodologie qui utilise, sans démontage avancé de la batterie, simultanément :
- La désulfatation électronique qui envoie des impulsions à la fréquence de résonance du sulfate de plomb supposées aider plus efficacement qu’une recharge normale, au retour du soufre dans la solution d’électrolyte sous forme ionique.
- La désulfatation chimique qui utilise un détergent pour retirer le sulfate de plomb des électrodes.
- La désulfatation mécanique qui par des remous de jets d’eau sous pression lavent les électrodes en retirant les agglomérats de sulfate de plomb. Notez que dans certains pays, les batteries au plomb sont réparées par démontage complet et brossage manuel ou remplacement des électrodes. Cela pose des questions d’hygiène et de sécurité liées à la manipulation du plomb.
Veuillez noter que, la sulfatation des électrodes fait partie du fonctionnement normal d’une batterie acide-plomb. C’est lorsque la présence de sulfate de plomb sur les électrodes est trop importante que la résistance interne de la batterie ne permet plus la circulation d’un courant susceptible de relancer le processus de charge (réduction sur la cathode, oxydation sur l’anode).

Ainsi la batterie ne fonctionne plus. Vous conclurez donc que, non seulement il ne faut jamais ajouter d’acide dans une batterie sulfatée, ce qui aurait pour conséquence de la saturer davantage en soufre, et que la première chose à tenter pour réparer une batterie n’est autre qu’une charge prolongée. La charge est en elle même le premier procédé de désulfatation.
Le procédé et son matériel associé
Schéma
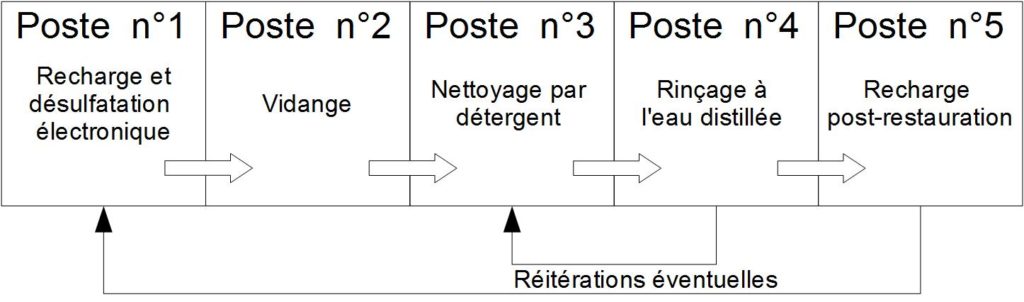
- Poste n°1 : La toute première action à tenter pour réparer une batterie est une charge prolongée. Avant de tenter une recharge, il faut s’assurer que le niveau d’eau dans les compartiments est suffisant. Si la batterie n’est pas munie de bouchons dévissables, il faudra desceller le ou les couvercle(s) afin d’accéder aux compartiments. Après avoir fait l’appoint avec de l’eau distillée exclusivement, une première tentative de charge longue est possible (une journée par exemple). Certaines batteries hors d’usage ont une résistance interne tellement élevée qu’elle ne permet même pas le démarrage du processus de recharge. Dans ce cas, une autre tentative est recommandée avant de poursuivre le processus. En ajoutant une solution de sulfate de magnésium heptahydraté (quantités à étudier) dans les compartiments, puis en secouant la batterie, la résistance interne peut diminuer suffisamment de telle sorte qu’un début de recharge est possible. Dans ce cas, il faut effectivement réaliser la tentative de recharge longue avant de poursuivre le processus. Pour les batterie totalement sulfatée, ce procédé reste malheureusement sans effets.
- Poste n°2 : Ce poste est physiquement constitué d’un bac de rétention pour futs industriels, résistant à l’acide sulfurique. Il permet de retourner directement les batteries en provenance du poste 1 (avec succès ou échec de la recharge longue) pour la vidanger. S’il est assez grand il pourra recueillir l’acide de plusieurs batteries. Il convient ensuite de récupérer cette solution puis de la filtrer à 20 microns (à l’aide d’un filtre en nylon). Elle sera réutilisée au poste 5 en corrigeant son taux d’acidité.
- Poste n°3 : A ce poste, les compartiments des batteries vides en provenance du poste 2 sont remplies avec une solution d’E.D.T.A. tétrasodique (à ne pas confondre avec l’E.D.T.A.). Il va se produire une réaction générant de la mousse, il convient de laisser la solution jusqu’à l’arrêt de l’effervescence. Le sulfate de plomb est dissout par le détergent. Vous remarquerez qu’en cas de sulfatation très prononcée, la dissolution du sulfate de plomb peut désagréger les électrodes et la batterie serait alors définitivement hors d’usage à moins de la reconstruire par démontage, ce qui n’est pas l’objet du procédé proposé. Ce poste n’est pas qu’un support avec un bac de rétention, il comporte aussi des injecteurs de nettoyage par remous. Lorsque deux batteries ou plus sont remplies de détergent, deux autres dont la réaction s’est arrêtée peuvent être lavées mécaniquement.
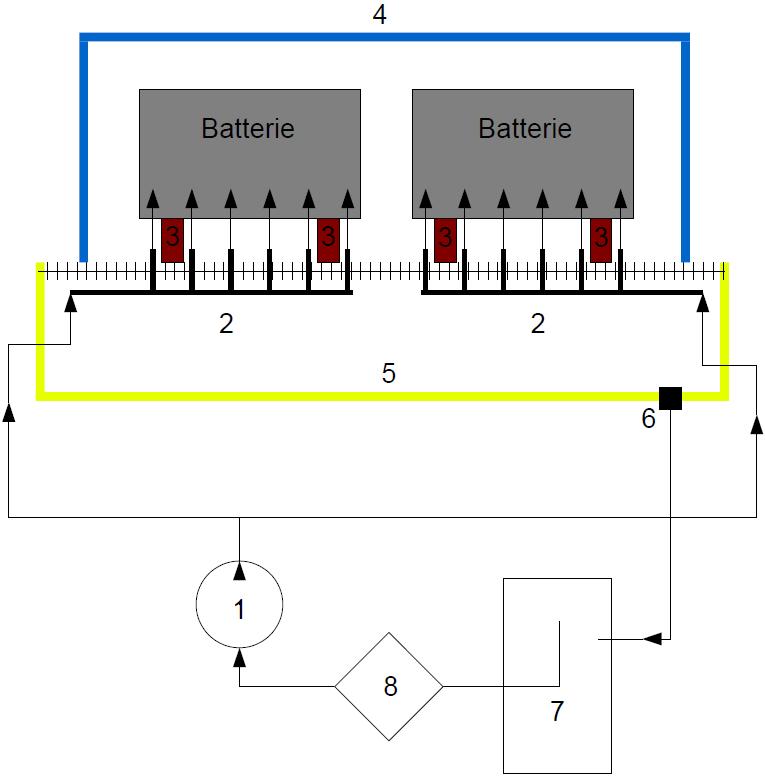
1. Pompe (pompe de lave-vaisselle par exemple, résistante à l'acide) 2. Rampes d'injecteurs 3. Supports des batteries 4. Bac en plastique 5. Bac de rétention 6. Passe-cloison en plastique (résistant à l'acide sulfurique) 7. Bac de décantation et de séparation des résidus par centrifugation 8. Filtre (résistant à l'acide)
- Poste n°4 : Ce poste est presque le même que le poste 3, si ce n’est que le circuit de pompage est ouvert et que le rinçage se fait en temps limité. Il est peut être possible d’utiliser de l’eau de pluie scrupuleusement filtrée pour remplacer l’eau distillée relativement coûteuse.
- Poste n°5 : Ici, les batteries sont remplies de nouveau avec l’électrolyte filtrée récupérée au poste 2. Il est recommandé d’utiliser une solution d’acide au degré inférieur à celui recommandé. Ce degré se déduit de la densité, mesurable avec un pèse acide (l’eau a une densité de 1kg/l). En effet, si du sulfate de plomb encombre encore les électrodes, le soufre qui le compose migrera de nouveau sous forme ionique dans l’électrolyte, ce n’est qu’après avoir rechargé une première fois la batterie que la densité pourra être corrigée (batterie chargée) pour atteindre environ 1.25 kg/l, après l’avoir secouée. Il faut également veiller à ce que le niveau d’électrolyte soit à son niveau normal. Si la densité est anormalement élevée après recharge, c’est sans doute que la batterie était encore partiellement sulfatée et que la recharge a retourné du soufre dans l’électrolyte. Dans ce cas, il faut retirer une partie de l’acide, corriger le niveau à l’eau distillée et poursuivre la charge. Il convient de réitérer cette opération tant que le phénomène est perceptible. Lorsqu’il n’y a plus d’évolution, vous pourrez corriger définitivement, batterie chargée, la quantité d’acide.
Conclusion
Si malgré ce processus une batterie refuse de se recharger, ne serait-ce qu’un peu, vous pouvez la considérer comme irrécupérable au regard des capacités de ce système. Si toutefois la batterie semble commencer à se désulfater, que du courant accepte d’y entrer avec une tension supérieure à 10.8v, alors vous pourrez tenter de réitérer l’opération du poste 1 seule, qui peut suffire, ou bien l’intégralité du procédé.
